In die gebied van moderne medisyne het antibiotika bewys dat dit een van die belangrikste vooruitgang is, wat die voorkoms en mortaliteitsyfers wat met mikrobiese infeksies verband hou, dramaties verlaag het. Hul vermoë om die kliniese uitkomste van bakteriële infeksies te verander, het die lewensverwagting van tallose pasiënte verleng. Antibiotika is van kritieke belang in komplekse mediese prosedures, insluitend chirurgie, inplantingsplasings, oorplantings en chemoterapie. Die opkoms van antibiotika-weerstandige patogene is egter 'n groeiende bron van kommer, wat die doeltreffendheid van hierdie middels mettertyd verminder. Gevalle van antibiotika-weerstand is in alle kategorieë antibiotika gedokumenteer namate mikrobiese mutasies voorkom. Die seleksiedruk wat deur antimikrobiese middels uitgeoefen word, het bygedra tot die opkoms van weerstandige stamme, wat 'n beduidende uitdaging vir globale gesondheid inhou.
Om die dringende kwessie van antimikrobiese weerstand te bekamp, is dit noodsaaklik om effektiewe infeksiebeheerbeleide te implementeer wat die verspreiding van weerstandige patogene beperk, asook die gebruik van antibiotika verminder. Verder is daar 'n dringende behoefte aan alternatiewe behandelingsmetodes. Hiperbariese suurstofterapie (HBOT) het in hierdie konteks na vore gekom as 'n belowende modaliteit, wat die inaseming van 100% suurstof teen spesifieke drukvlakke vir 'n tydperk behels. Geposisioneer as 'n primêre of komplementêre behandeling vir infeksies, kan HBOT nuwe hoop bied in die behandeling van akute infeksies wat deur antibiotika-weerstandige patogene veroorsaak word.
Hierdie terapie word toenemend toegepas as 'n primêre of alternatiewe behandeling vir verskeie toestande, insluitend inflammasie, koolstofmonoksiedvergiftiging, chroniese wonde, iskemiese siektes en infeksies. Die kliniese toepassings van HBOT in infeksiebehandeling is diepgaande en bied onskatbare voordele vir pasiënte.

Kliniese Toepassings van Hiperbariese Suurstofterapie in Infeksie
Huidige bewyse ondersteun die toepassing van HBOT sterk, beide as 'n alleenstaande en aanvullende behandeling, wat beduidende voordele vir besmette pasiënte bied. Tydens HBOT kan die arteriële bloedsuurstofdruk tot 2000 mmHg styg, en die gevolglike hoë suurstof-weefseldrukgradiënt kan weefselsuurstofvlakke tot 500 mmHg verhoog. Sulke effekte is veral waardevol in die bevordering van die genesing van inflammatoriese reaksies en mikrosirkulasie-ontwrigtings wat in iskemiese omgewings waargeneem word, sowel as in die bestuur van kompartementsindroom.
HBOT kan ook toestande beïnvloed wat afhanklik is van die immuunstelsel. Navorsing dui daarop dat HBOT outo-immuun sindrome en antigeen-geïnduseerde immuunresponse kan onderdruk, wat help om oorplantingstoleransie te handhaaf deur die sirkulasie van limfosiete en leukosiete te verminder terwyl dit immuunresponse moduleer. Daarbenewens kan HBOTondersteun genesingin chroniese velletsels deur angiogenese te stimuleer, 'n kritieke proses vir verbeterde herstel. Hierdie terapie moedig ook die vorming van kollageenmatriks aan, 'n noodsaaklike fase in wondgenesing.
Spesiale aandag moet gegee word aan sekere infeksies, veral diep en moeilik behandelbare infeksies soos nekrotiserende fasciitis, osteomielitis, chroniese sagteweefselinfeksies en aansteeklike endokarditis. Een van die mees algemene kliniese toepassings van HBOT is vir vel-sagteweefselinfeksies en osteomielitis wat verband hou met lae suurstofvlakke wat dikwels deur anaërobiese of weerstandige bakterieë veroorsaak word.
1. Diabetiese voetinfeksies
Diabetiese voetMaagsere is 'n algemene komplikasie onder diabetiese pasiënte wat tot 25% van hierdie bevolking affekteer. Infeksies ontstaan gereeld in hierdie maagsere (wat 40%-80% van gevalle uitmaak) en lei tot verhoogde morbiditeit en mortaliteit. Diabetiese voetinfeksies (DFI's) bestaan gewoonlik uit polimikrobiese infeksies met 'n verskeidenheid anaërobiese bakteriële patogene wat geïdentifiseer is. Verskeie faktore, insluitend fibroblastfunksiedefekte, kollageenvormingsprobleme, sellulêre immuunmeganismes en fagosietfunksie, kan wondgenesing by diabetiese pasiënte belemmer. Verskeie studies het verswakte veloksigenasie as 'n sterk risikofaktor vir amputasies wat verband hou met DFI's geïdentifiseer.
As een van die huidige opsies vir DFI-behandelingDaar is berig dat HBOT die genesingstempo vir diabetiese voetswere aansienlik verhoog, wat gevolglik die behoefte aan amputasies en ingewikkelde chirurgiese ingrypings verminder. Dit verminder nie net die noodsaaklikheid van hulpbron-intensiewe prosedures, soos flapoperasies en veloorplantings nie, maar bied ook laer koste en minimale newe-effekte in vergelyking met chirurgiese opsies. 'n Studie deur Chen et al. het getoon dat meer as 10 sessies van HBOT gelei het tot 'n verbetering van 78,3% in wondgenesingstempo's by diabetiese pasiënte.
2. Nekrotiserende sagteweefselinfeksies
Nekrotiserende sagteweefselinfeksies (NSTI's) is dikwels polimikrobies, tipies ontstaan uit 'n kombinasie van aërobiese en anaërobiese bakteriële patogene en word dikwels geassosieer met gasproduksie. Terwyl NSTI's relatief skaars is, toon hulle 'n hoë mortaliteitsyfer as gevolg van hul vinnige progressie. Tydige en gepaste diagnose en behandeling is die sleutel tot die bereiking van gunstige uitkomste, en HBOT is aanbeveel as 'n aanvullende metode vir die bestuur van NSTI's. Alhoewel daar steeds twis is oor die gebruik van HBOT in NSTI's weens die gebrek aan prospektiewe beheerde studies,Bewyse dui daarop dat dit moontlik gekorreleer kan wees met verbeterde oorlewingsyfers en orgaanbewaring in NSTI-pasiënte'n Retrospektiewe studie het 'n beduidende vermindering in mortaliteitsyfers onder NSTI-pasiënte wat HBOT ontvang, aangedui.
1.3 Infeksies van die chirurgiese plek
SSI's kan geklassifiseer word op grond van die anatomiese plek van die infeksie en kan ontstaan as gevolg van verskeie patogene, insluitend beide aërobiese en anaërobiese bakterieë. Ten spyte van vooruitgang in infeksiebeheermaatreëls, soos sterilisasietegnieke, die gebruik van profilaktiese antibiotika en verbeterings in chirurgiese praktyke, bly SSI's 'n aanhoudende komplikasie.
Een beduidende oorsig het die doeltreffendheid van HBOT in die voorkoming van diep SSI's in neuromuskulêre skoliose-chirurgie ondersoek. Preoperatiewe HBOT kan die voorkoms van SSI's aansienlik verminder en wondgenesing vergemaklik. Hierdie nie-indringende terapie skep 'n omgewing waar suurstofvlakke in die wondweefsel verhoog is, wat geassosieer word met die oksidatiewe doodmaakaksie teen patogene. Daarbenewens spreek dit die verlaagde bloed- en suurstofvlakke aan wat bydra tot die ontwikkeling van SSI's. Benewens ander infeksiebeheerstrategieë, is HBOT veral aanbeveel vir skoon-besmette operasies soos kolorektale prosedures.
1.4 Brandwonde
Brandwonde is beserings wat veroorsaak word deur uiterste hitte, elektriese stroom, chemikalieë of bestraling en kan hoë morbiditeits- en mortaliteitsyfers inhou. HBOT is voordelig in die behandeling van brandwonde deur die suurstofvlakke in beskadigde weefsels te verhoog. Terwyl diere- en kliniese studies gemengde resultate toon rakendedie doeltreffendheid van HBOT in brandbehandeling, 'n Studie met 125 brandwondpasiënte het aangedui dat HBOT geen beduidende impak op mortaliteitsyfers of die aantal operasies wat uitgevoer is, getoon het nie, maar wel die gemiddelde genesingstyd verminder het (19,7 dae in vergelyking met 43,8 dae). Die integrasie van HBOT met omvattende brandwondbestuur kan sepsis by brandwondpasiënte effektief beheer, wat lei tot korter genesingstye en verminderde vloeistofbehoeftes. Verdere uitgebreide prospektiewe navorsing is egter nodig om die rol van HBOT in die bestuur van uitgebreide brandwonde te bevestig.
1.5 Osteomielitis
Osteomielitis is 'n infeksie van die been of beenmurg wat dikwels deur bakteriële patogene veroorsaak word. Die behandeling van osteomielitis kan uitdagend wees as gevolg van die relatief swak bloedtoevoer na bene en die beperkte penetrasie van antibiotika in die murg. Chroniese osteomielitis word gekenmerk deur aanhoudende patogene, ligte inflammasie en nekrotiese beenweefselvorming. Refraktêre osteomielitis verwys na chroniese beeninfeksies wat voortduur of terugkeer ten spyte van toepaslike behandeling.
Daar is getoon dat HBOT die suurstofvlakke in die besmette beenweefsel aansienlik verbeter. Talle gevallestudies en kohortstudies dui daarop dat HBOT kliniese uitkomste vir osteomielitis-pasiënte verbeter. Dit blyk deur verskeie meganismes te werk, insluitend die bevordering van metaboliese aktiwiteit, die onderdrukking van bakteriële patogene, die verbetering van antibiotiese effekte, die minimalisering van inflammasie en die bevordering van genesing.prosesse. Na HBOT toon 60% tot 85% van pasiënte met chroniese, refraktêre osteomielitis tekens van infeksieonderdrukking.
1.6 Swaminfeksies
Wêreldwyd ly meer as drie miljoen individue aan chroniese of indringende swaminfeksies, wat jaarliks tot meer as 600 000 sterftes lei. Behandelingsuitkomste vir swaminfeksies word dikwels benadeel as gevolg van faktore soos veranderde immuunstatus, onderliggende siektes en patogeen-virulensie-eienskappe. HBOT word 'n aantreklike terapeutiese opsie in ernstige swaminfeksies as gevolg van die veiligheid en nie-indringende aard daarvan. Studies dui daarop dat HBOT effektief kan wees teen swampatogene soos Aspergillus en Mycobacterium tuberculosis.
HBOT bevorder antifungale effekte deur die biofilmvorming van Aspergillus te inhibeer, met verhoogde doeltreffendheid wat opgemerk word in stamme wat superoksied dismutase (SOD) gene kort. Die hipoksiese toestande tydens swaminfeksies bied uitdagings vir die aflewering van antifungale middels, wat die verhoogde suurstofvlakke van HBOT 'n potensieel voordelige intervensie maak, hoewel verdere navorsing geregverdig is.
Die antimikrobiese eienskappe van HBOT
Die hiperoksiese omgewing wat deur HBOT geskep word, inisieer fisiologiese en biochemiese veranderinge wat antibakteriese eienskappe stimuleer, wat dit 'n effektiewe aanvullende terapie vir infeksie maak. HBOT toon merkwaardige effekte teen aërobiese bakterieë en hoofsaaklik anaërobiese bakterieë deur meganismes soos direkte bakteriedodende aktiwiteit, verbetering van immuunresponse en sinergistiese effekte met spesifieke antimikrobiese middels.
2.1 Direkte antibakteriese effekte van HBOT
Die direkte antibakteriese effek van HBOT word grootliks toegeskryf aan die generering van reaktiewe suurstofspesies (ROS), wat superoksiedanione, waterstofperoksied, hidroksielradikale en hidroksielione insluit - wat almal tydens sellulêre metabolisme ontstaan.
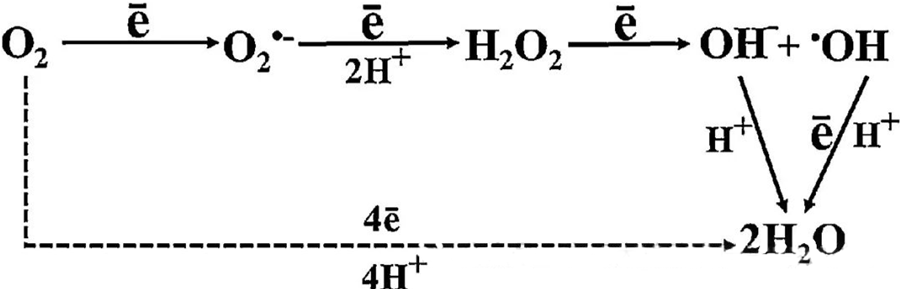
Die interaksie tussen O₂ en sellulêre komponente is noodsaaklik om te verstaan hoe ROS binne selle vorm. Onder sekere toestande, wat oksidatiewe stres genoem word, word die balans tussen ROS-vorming en die afbraak daarvan ontwrig, wat lei tot verhoogde vlakke van ROS in selle. Die produksie van superoksied (O₂⁻) word gekataliseer deur superoksieddismutase, wat vervolgens O₂⁻ in waterstofperoksied (H₂O₂) omskakel. Hierdie omskakeling word verder versterk deur die Fenton-reaksie, wat Fe²⁺ oksideer om hidroksielradikale (·OH) en Fe³⁺ te genereer, wat sodoende 'n nadelige redoksvolgorde van ROS-vorming en sellulêre skade begin.
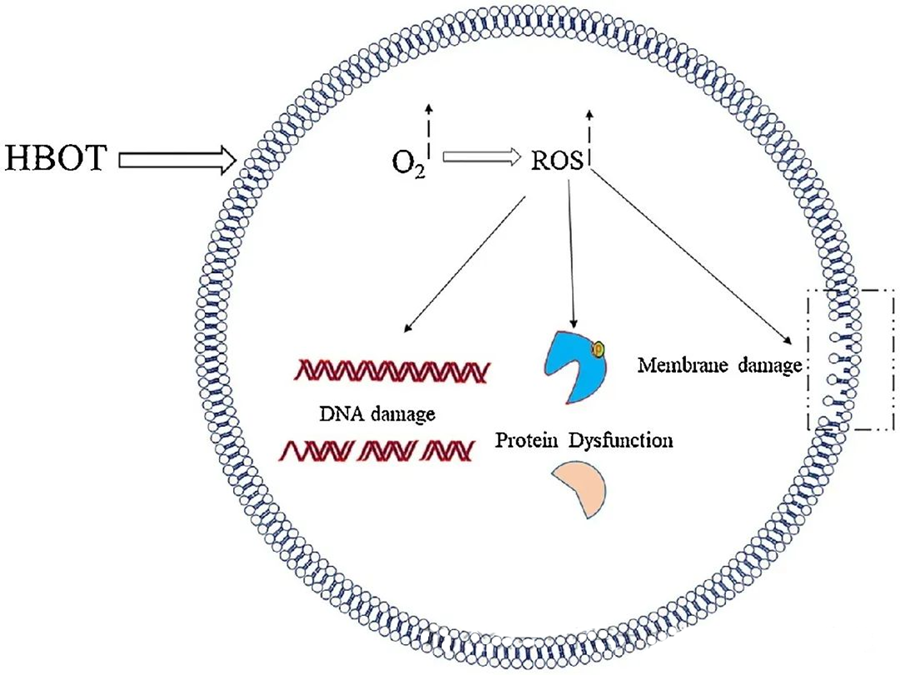
Die toksiese effekte van ROS teiken kritieke sellulêre komponente soos DNS, RNS, proteïene en lipiede. Dit is opmerklik dat DNS 'n primêre teiken van H₂O₂-gemedieerde sitotoksisiteit is, aangesien dit deoksiribosestrukture ontwrig en basissamestellings beskadig. Die fisiese skade wat deur ROS veroorsaak word, strek tot die heliksstruktuur van DNS, moontlik as gevolg van lipiedperoksidasie wat deur ROS veroorsaak word. Dit beklemtoon die nadelige gevolge van verhoogde ROS-vlakke binne biologiese stelsels.
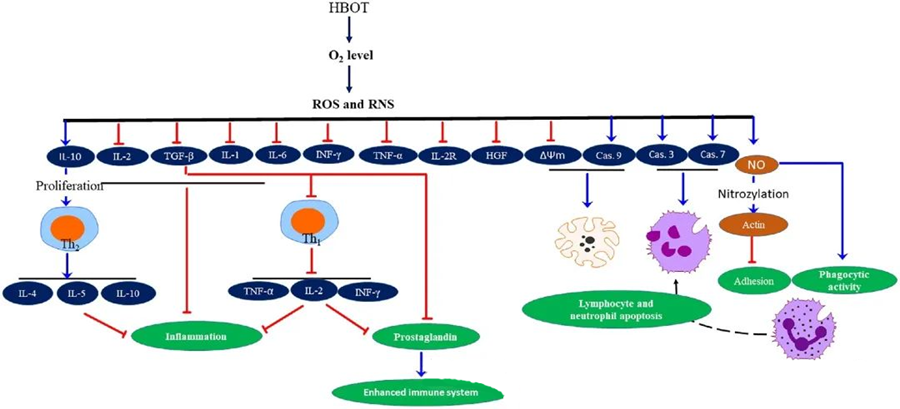
Antimikrobiese Werking van ROS
ROS speel 'n belangrike rol in die inhibering van mikrobiese groei, soos gedemonstreer deur HBOT-geïnduseerde ROS-generering. Die toksiese effekte van ROS teiken direk sellulêre bestanddele soos DNS, proteïene en lipiede. Hoë konsentrasies aktiewe suurstofspesies kan lipiede direk beskadig, wat lei tot lipiedperoksidasie. Hierdie proses kompromitteer die integriteit van selmembrane en gevolglik die funksionaliteit van membraan-geassosieerde reseptore en proteïene.
Verder ondergaan proteïene, wat ook belangrike molekulêre teikens van ROS is, spesifieke oksidatiewe modifikasies by verskeie aminosuurresidue soos sisteïen, metionien, tirosien, fenielalanien en triptofaan. Daar is byvoorbeeld getoon dat HBOT oksidatiewe veranderinge in verskeie proteïene in E. coli veroorsaak, insluitend verlengingsfaktor G en DnaK, wat sodoende hul sellulêre funksies beïnvloed.
Verbetering van immuniteit deur HBOT
Die anti-inflammatoriese eienskappe van HBOTis gedokumenteer, wat noodsaaklik is vir die verligting van weefselskade en die onderdrukking van infeksieprogressie. HBOT beïnvloed die uitdrukking van sitokiene en ander inflammatoriese reguleerders beduidend, wat die immuunrespons beïnvloed. Verskeie eksperimentele stelsels het differensiële veranderinge in geenuitdrukking en proteïengenerering na HBOT waargeneem, wat groeifaktore en sitokiene óf opreguleer óf afreguleer.
Tydens die HBOT-proses veroorsaak verhoogde O₂-vlakke 'n reeks sellulêre reaksies, soos die onderdrukking van die vrystelling van pro-inflammatoriese mediators en die bevordering van limfosiet- en neutrofiel-apoptose. Gesamentlik verbeter hierdie aksies die immuunstelsel se antimikrobiese meganismes, wat die genesing van infeksies vergemaklik.
Verder dui studies daarop dat verhoogde O₂-vlakke tydens HBOT die uitdrukking van pro-inflammatoriese sitokiene, insluitend interferon-gamma (IFN-γ), interleukien-1 (IL-1) en interleukien-6 (IL-6), kan verminder. Hierdie veranderinge sluit ook die afregulering van die verhouding van CD4:CD8 T-selle en die modulering van ander oplosbare reseptore in, wat uiteindelik interleukien-10 (IL-10) vlakke verhoog, wat noodsaaklik is om inflammasie teen te werk en genesing te bevorder.
Die antimikrobiese aktiwiteite van HBOT is verweef met komplekse biologiese meganismes. Daar is berig dat beide superoksied en verhoogde druk HBOT-geïnduseerde antibakteriese aktiwiteit en neutrofiel-apoptose op 'n inkonsekwente wyse bevorder. Na HBOT verbeter 'n merkbare toename in suurstofvlakke die bakteriedodende vermoëns van neutrofiele, 'n noodsaaklike komponent van die immuunrespons. Verder onderdruk HBOT neutrofieladhesie, wat gemedieer word deur die interaksie van β-integrine op neutrofiele met intersellulêre adhesiemolekules (ICAM) op endoteelselle. HBOT inhibeer die aktiwiteit van neutrofiel β-2-integrine (Mac-1, CD11b/CD18) deur 'n stikstofoksied (NO)-gemedieerde proses, wat bydra tot die migrasie van neutrofiele na die plek van infeksie.
Die presiese herrangskikking van die sitoskelet is nodig vir neutrofiele om patogene effektief te fagositiseer. Daar is getoon dat S-nitrosilering van aktien aktienpolimerisasie stimuleer, wat moontlik die fagositiese aktiwiteit van neutrofiele na HBOT-voorbehandeling vergemaklik. Boonop bevorder HBOT apoptose in menslike T-sellyne deur mitochondriale bane, met versnelde limfosietdood na HBOT wat gerapporteer word. Die blokkering van kaspase-9 – sonder om kaspase-8 te beïnvloed – het die immunomodulerende effekte van HBOT gedemonstreer.
Die sinergistiese effekte van HBOT met antimikrobiese middels
In kliniese toepassings word HBOT gereeld saam met antibiotika gebruik om infeksies effektief te bestry. Die hiperoksiese toestand wat tydens HBOT bereik word, kan die doeltreffendheid van sekere antibiotiese middels beïnvloed. Navorsing dui daarop dat spesifieke bakteriedodende middels, soos β-laktame, fluorokinolone en aminoglikosiede, nie net deur inherente meganismes werk nie, maar ook gedeeltelik staatmaak op die aërobiese metabolisme van bakterieë. Daarom is die teenwoordigheid van suurstof en die metaboliese eienskappe van patogene deurslaggewend wanneer die terapeutiese effekte van antibiotika geëvalueer word.
Beduidende bewyse het getoon dat lae suurstofvlakke die weerstand van Pseudomonas aeruginosa teen piperacillin/tazobactam kan verhoog en dat 'n lae suurstofomgewing ook bydra tot die verhoogde weerstand van Enterobacter cloacae teen azitromisien. Omgekeerd kan sekere hipoksiese toestande bakteriële sensitiwiteit vir tetrasiklien-antibiotika verhoog. HBOT dien as 'n lewensvatbare aanvullende terapeutiese metode deur aërobiese metabolisme te induseer en hipoksies-besmette weefsels te heroksigeneer, wat gevolglik die sensitiwiteit van patogene vir antibiotika verhoog.
In prekliniese studies het die kombinasie van HBOT—twee keer per dag vir 8 uur teen 280 kPa toegedien—saam met tobramisien (20 mg/kg/dag) die bakteriese ladings in Staphylococcus aureus-infektiewe endokarditis aansienlik verminder. Dit demonstreer die potensiaal van HBOT as 'n aanvullende behandeling. Verdere ondersoeke het aan die lig gebring dat HBOT onder 37°C en 3 ATA-druk vir 5 uur die effekte van imipenem teen makrofaag-geïnfekteerde Pseudomonas aeruginosa aansienlik versterk het. Daarbenewens is gevind dat die gekombineerde modaliteit van HBOT met cefasolin meer effektief is in die behandeling van Staphylococcus aureus-osteomielitis in diermodelle in vergelyking met cefasolin alleen.
HBOT verhoog ook die bakteriedodende werking van siprofloksasien teen Pseudomonas aeruginosa-biofilms aansienlik, veral na 90 minute se blootstelling. Hierdie verbetering word toegeskryf aan die vorming van endogene reaktiewe suurstofspesies (ROS) en toon verhoogde sensitiwiteit in peroksidase-defekte mutante.
In modelle van pleuritis veroorsaak deur metisillien-weerstandige Staphylococcus aureus (MRSA), het die gesamentlike effek van vankomisien, teikoplanien en linezolid met HBOT beduidend verhoogde doeltreffendheid teen MRSA getoon. Metronidasool, 'n antibiotikum wat wyd gebruik word in die behandeling van ernstige anaërobiese en polimikrobiese infeksies soos diabetiese voetinfeksies (DFI's) en chirurgiese plekinfeksies (SSI's), het hoër antimikrobiese doeltreffendheid onder anaërobiese toestande getoon. Toekomstige studies is geregverdig om die sinergistiese antibakteriese effekte van HBOT gekombineer met metronidasool in beide in vivo en in vitro omgewings te ondersoek.
Die antimikrobiese doeltreffendheid van HBOT op weerstandbiedende bakterieë
Met die evolusie en verspreiding van weerstandige stamme verloor tradisionele antibiotika dikwels hul sterkte mettertyd. Verder kan HBOT noodsaaklik wees in die behandeling en voorkoming van infeksies wat veroorsaak word deur multidwelm-weerstandige patogene, wat dien as 'n kritieke strategie wanneer antibiotiese behandelings misluk. Talle studies het die beduidende bakteriedodende effekte van HBOT op klinies relevante weerstandige bakterieë gerapporteer. Byvoorbeeld, 'n 90-minuut HBOT-sessie teen 2 OTM het die groei van MRSA aansienlik verminder. Daarbenewens het HBOT in verhoudingsmodelle die antibakteriese effekte van verskeie antibiotika teen MRSA-infeksies verbeter. Verslae het bevestig dat HBOT effektief is in die behandeling van osteomielitis wat veroorsaak word deur OXA-48-produserende Klebsiella pneumoniae sonder dat enige bykomende antibiotika nodig is.
Kortliks, hiperbariese suurstofterapie verteenwoordig 'n veelsydige benadering tot infeksiebeheer, wat die immuunrespons verbeter terwyl dit ook die doeltreffendheid van bestaande antimikrobiese middels versterk. Met omvattende navorsing en ontwikkeling hou dit die potensiaal in om die gevolge van antibiotika-weerstandigheid te versag, wat hoop bied in die voortdurende stryd teen bakteriële infeksies.
Plasingstyd: 28 Februarie 2025

